原创 奇点糕 奇点网 收录于话题#二甲双胍 31 个 #奇点网 87 个

降糖、抗衰、抗癌遇瓶颈,怎么办?
你为何不问问神奇的二甲双胍呢?

二甲双胍作为降糖药,已经为2型糖尿病患者“服务”了几十年了,也是目前世界上应用最广泛的降糖药物[1]。
除了能降糖,近年来,二甲双胍还被陆续发现各种其他潜在功效,比如降低胆固醇、抗衰延寿、抗癌等。广泛的应用、便宜的价格,妥妥的平民战神,让不少人直呼“我可以!”(这里必须处方药警告)。
不过,这位平民战神虽说是战果累累,但关于其作用靶点仍是众说纷纭。
目前的研究表明,二甲双胍可直接作用于肝脏、肾脏和肠道,在转运入细胞后,主要通过激活AMPK信号通路来发挥降糖等重要生物学功能[2,3]。这个AMPK可是人体代谢的总开关,在细胞能量稳态调节中起重要作用。但要细问二甲双胍是如何打开这个开关的,这中间的关键靶点以及相关机制还真说不清楚。
厦门大学的林圣彩院士团队与邓贤明团队联手合作,为我们拨开了二甲双胍的靶点疑云,进一步揭示二甲双胍的作用机制[4]。
他们发现,一种名为PEN2的蛋白质是关键靶点。二甲双胍在与PEN2发生互作后,会抑制溶酶体质子泵v-ATPase的活性,从而激活AMPK信号通路,发挥降低葡萄糖水平、降低肝脏脂肪含量、延长寿命的功效。
文章于昨日发表在顶刊《自然》上。

论文首页截图
在研究二甲双胍激活AMPK的机制时,科学家们发现一个奇怪的现象。
作为真核细胞中高度保守的、最重要的能量感受器,AMPK可以感知细胞内葡萄糖水平的变化,当AMP/ATP 、ADP/ATP比率增加时被激活。换句话说,二甲双胍要想打开AMPK这个开关,得先让细胞内AMP/ATP 、ADP/ATP的比率波动起来才行[5,6]。
然而,这种变化只能在小鼠的大剂量口服实验中观察到[7]。有研究表明,临床上患者在使用二甲双胍治疗时,血液中的二甲双胍浓度并不足以引起细胞中AMP/ATP和ADP/ATP比率出现增加,可是二甲双胍的疗效还好好的[3]。
这样一来,激活AMPK的典型途径并不完全适用于二甲双胍,二甲双胍可能不走寻常路,以一条全新的、不依赖于AMP的通路用来激活AMPK。
对此,2017年时,林圣彩院士团队提出了溶酶体通路,并命名为“林通路”。他们认为,二甲双胍正是以这条不依赖于AMP的通路来激活AMPK的,这为二甲双胍甚至AMPK的相关机制研究都指出了一个新方向,只是未能完全揭示溶酶体通路的全貌[8]。
经过研究团队的不懈探索,拨开层层迷雾,如今二甲双胍的溶酶体通路终于由他们亲手补上关键一笔。
那就赶紧一起来看看,此次林圣彩院士团队与邓贤明团队是如何找到这个分子靶点的吧。
首先,也是此次研究中的重头戏——钓鱼。
此钓鱼非彼钓鱼,是指分子探针技术,可用于研究与特定靶分子之间发生的特异性相互作用。使这个法子来钓神秘靶点,再合适不过了。
研究者们经过一系列摸索后,成功合成二甲双胍的分子探针(Met-P),与溶酶体的蛋白质提取物进行孵育。在溶酶体这个池塘里,以二甲双胍为饵,引未知靶点分子这条鱼上钩,由生物素分子这根竿完成收线,将二甲双胍-蛋白质复合物一并收回。再通过质谱等方法,共在溶酶体蛋白质提取物中筛选得到113种与二甲双胍发生特异性结合的蛋白质。
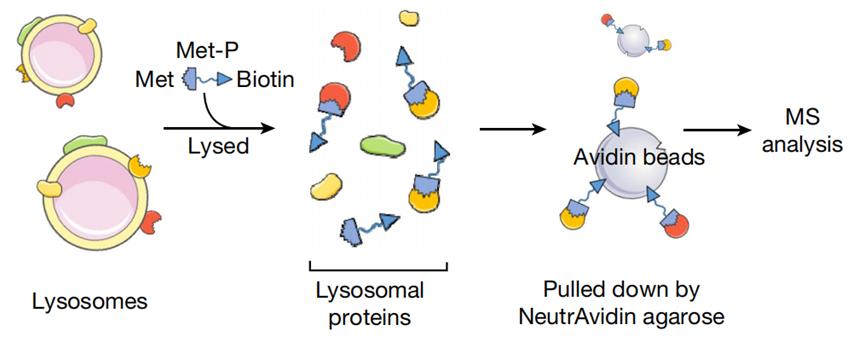
钓,啥都能钓
但钓鱼人都懂一件事,那便是钓获放流、只取所需。
此次,研究者们一心所求的,就是那个在二甲双胍激活AMPK通路中起关键作用的靶点。其余的蛋白质和二甲双胍发生结合后干了点儿啥,这是另外的价钱就交给后续研究了。
他们在小鼠胚胎成纤维细胞、人原代肝细胞中,分别敲低这113种蛋白质的表达,进行体外培养,并观察哪种蛋白质的表达能够调控二甲双胍对细胞内AMPK分子的激活作用。
结果显示,PEN2蛋白质就是研究者们真正要找的鱼,是二甲双胍启动溶酶体通路、激活AMPK的关键靶点。
当PEN2表达被敲低或是Pen2基因被敲除时,二甲双胍对细胞内AMPK信号通路的激活作用就会被抑制。并鉴定出PEN2上与二甲双胍相关的关键活性位点F35和E40。
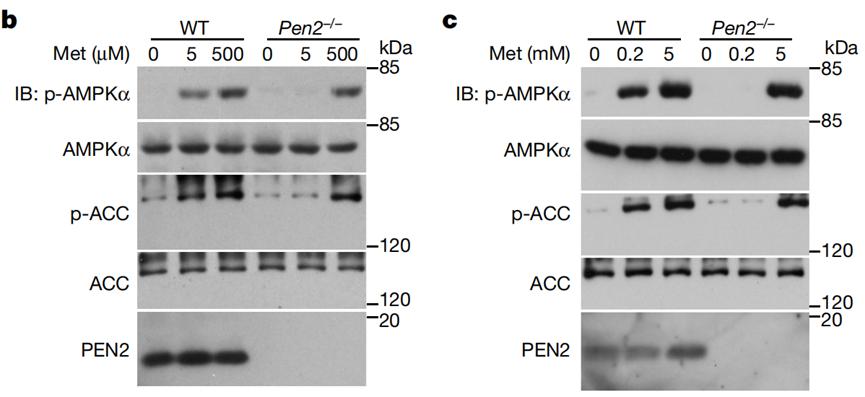
PEN2表达敲除时,二甲双胍在低剂量情况下就无法激活AMPK
研究者们进一步在动物体内实验中证实了PEN2的身份。
他们将小鼠、秀丽隐杆线虫的PEN2敲除后发现,二甲双胍无法再激活AMPK,而且二甲双胍诱导的降低葡萄糖水平、降低肝脏脂肪含量、寿命延长的效果也都无了。这些足以说明,PEN2在二甲双胍的作用机制中是个不可或缺的信号分子。
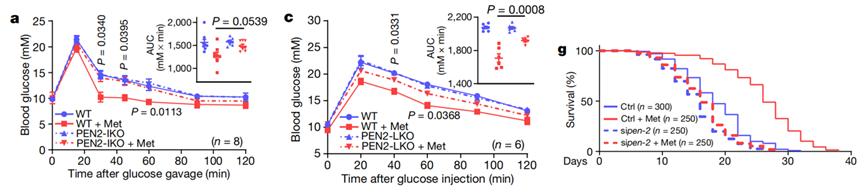
a、c、g:依次为二甲双胍诱导的降低葡萄糖水平、降低肝脏脂肪含量、寿命延长的效果
最后,从机制上来看,二甲双胍在转入细胞并与PEN2发生结合之后,诱导PEN2与v-ATPase的一个亚基——ATP6AP1结合并形成复合物,从而抑制v-ATPase的活性。一旦v-ATPase的活性被抑制,AMPK信号通路即被激活。
综上所述,林圣彩院士团队与邓贤明团队联手发现了二甲双胍的关键分子靶点——PEN2。二甲双胍与PEN2结合后启动信号通路,通过ATP6AP1激活溶酶体的“葡萄糖传感器”AMPK,进而发挥降低葡萄糖水平、降低肝脏脂肪含量、延长寿命等功效。
对此,研究者们还特意强调道,这条通路不依赖于AMP,不会使细胞内AMP/ADP 水平发生扰动,这或许可以解释为什么二甲双胍在发挥其治疗益处的同时还不会有明显的副作用。
二甲双胍的机制还有很多未解之谜,真不知道这位平民战神到底还有哪些“神力”呢?
参考文献:
[1]Bailey CJ, Day C. Metformin: its botanical background. Practical Diabetes International. 2004;21(3):115–7. doi:10.1002/pdi.606
[2]Foretz, M., Guigas, B., Bertrand, L., Pollak, M. & Viollet, B. Metformin: from mechanisms of
action to therapies. Cell Metab. 20, 953–966 (2014).
[3]Graham, G. G. et al. Clinical pharmacokinetics of metformin. Clin. Pharmacokinet. 50,
81–98 (2011).
[4]https://www.nature.com/articles/s41586-022-04431-8
[5]El-Mir, M. Y. et al. Dimethylbiguanide inhibits cell respiration via an indirect effect targeted
on the respiratory chain complex I. J. Biol. Chem. 275, 223–228 (2000).
[6]Owen, M. R., Doran, E. & Halestrap, A. P. Evidence that metformin exerts its anti-diabetic
effects through inhibition of complex 1 of the mitochondrial respiratory chain. Biochem. J.
348, 607–614 (2000).
[7]Hunter, R. W. et al. Metformin reduces liver glucose production by inhibition of fructose-1-
6-bisphosphatase. Nat. Med. 24, 1395–1406 (2018).
[8]Zhang CS, et al. Fructose-1,6-bisphosphate and aldolase mediate glucose sensing by AMPK. Nature. 2017 Aug 3;548(7665):112-116. doi: 10.1038/nature23275. Epub 2017 Jul 19.

