正电子发射断层扫描仪(Positron Emission Tomography, PET)是当前医学界公认的肿瘤、心脏、脑等疾病诊断与病理生理研究的重要方法。随着核医学影像设备的广泛应用和计算机技术的迅速发展,图像重建方法作为PET成像的一个关键环节,其研究工作也越发受到重视。
PET探测器检测注入人体的示踪剂在湮灭辐射过程中产生的射线,经过符合采集系统处理形成投影线,以SINO的方式存放于计算机硬盘中[1]。计算机调用图像重建模块,生成人体断层图像。目前,PET图像基础重建算法主要包括解析法和迭代法。
1. 解析法
解析法是以中心切片定理为基础的反投影方法,常用的是滤波反投影法(Filtered Back-Projection, FBP)。在FBP中,图像重建主要包含两个步骤:反投影和滤波。
我们在初中就已经学过投影与反投影的概念,从不同角度观察物体可以得到不同的信息,当我们从多种不同角度获取物体的投影,可以反向推出这个物体真实的形态。
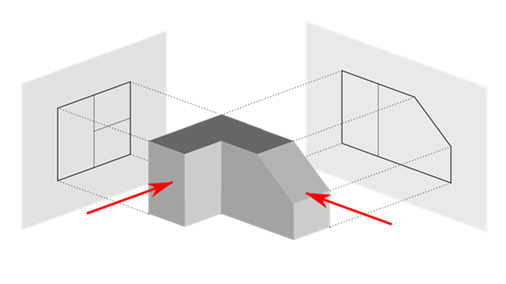
图1 光线将物体的形状投射到一个平面称为投影
在成像原理上,PET和CT略有差异。CT是投射成像,X射线旋转360°,采集被扫描物体不同角度的投影信息,通过反投影得到被扫描物体的结构信息。PET是发射成像,放射性药物从人体内发出不同角度的射线,探头实时探测放射性药物在不同角度的投影信息,通过反投影获得放射性药物在被扫描物体内的分布情况。
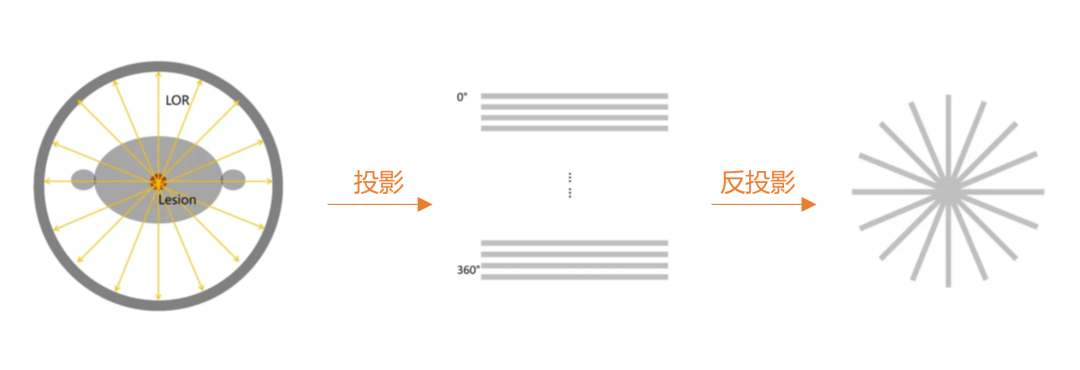
图2 PET探测器采集不同角度投影数据,通过反投影还原位置信息
通过反投影线的交点,我们可以确定信号的位置,但是会在信号周围产生星状伪影。因此,我们就需要通过滤波的方法来去除这些伪影,还原信号的真实分布情况。
在滤波中,如果对高频信号不做抑制,截止频率高,此时空间分辨最好,但所重建的图像不平滑,易产生振荡和高频伪影;反之,采用较低截止频率,过多压抑高频成分的低通窗函数会造成重建图像的模糊,故在滤波反投影法中低噪声和高分辨对滤波器的要求是矛盾的,需折中选择。滤波常用的窗函数有Hanning窗、Hamming窗、Butterworth窗、以及Shepp-Logan窗。
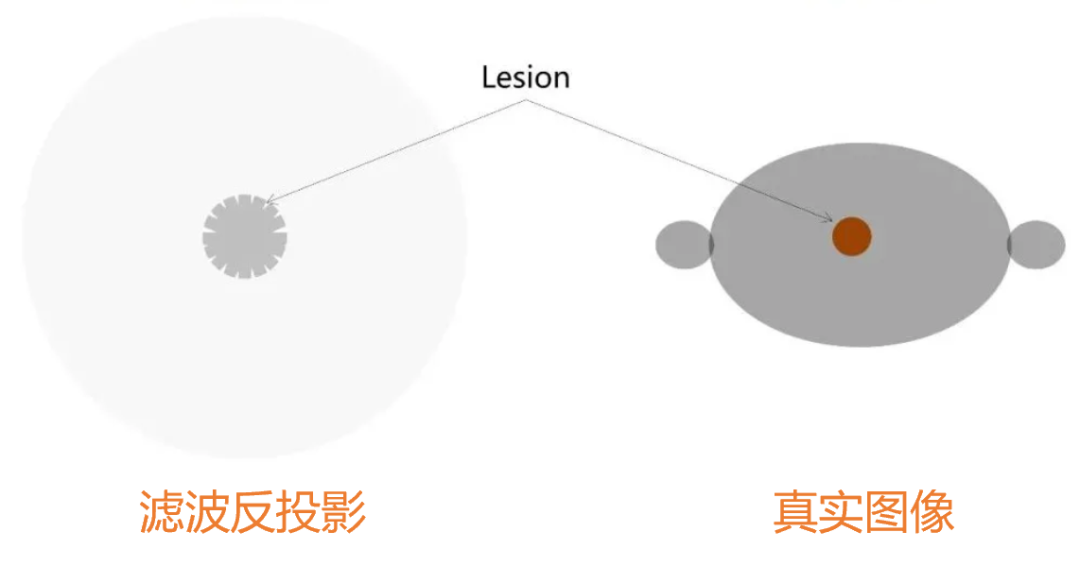
图3 滤波抑制星状伪影
投影数据越多,对放射信号的定位越精准,得到的图像质量也越高。FBP重建算法的优点是操作简便,易于临床实现,但是抗噪声能力差,在采集数据为相对欠采样和热源尺寸较小(如小病灶)的情况下,往往难以得到令人满意的重建图像。CT常规使用FBP进行图像重建,但PET考虑到数据量因素,通常较少在临床中使用此方法。
2. 迭代法
由于上述FBP重建法的缺点,迭代法应运而生。迭代法是从一幅假设的初始图像出发,采用逐步逼近的方法,将理论投影值同实际测量投影值进行比较,在某种最优化准则指导下寻找最优解。简单来说,迭代法就像我们有了一副人像画和一块橡皮泥,我们通过不断地比对照片,用橡皮泥还原人像的过程。
PET常用的迭代法有最大似然法(Maximum Likelihood Expectation-Maximization, MLEM )和有序子集最大似然法( Ordered Subset Expectation Maximization, OSEM)。
MLEM法首先假定一初始图像,计算该图像投影,与测量投影值对比,计算校正系数并更新初始图像值,满足停止规则时,迭代中止,否则以新的重建图像作为初始图像重复上述步骤。实际过程中受噪声、物理因素等影响,我们无法通过多次重复这一步骤完美的还原图像,因此需要设定一个迭代规则,得到最优解,即终止迭代[2]。
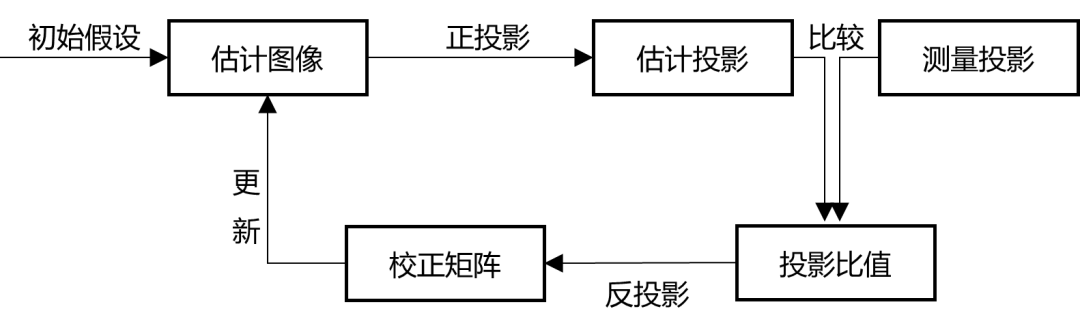
图4 迭代过程
与FBP重建相比较,在相对欠采样、低计数的PET成像中,MLEM迭代法得到的图像质量更好,图像分辨率更高。但是这种方法需要大量的计算,收敛速度很慢,所以就有了我们现在熟知的OSEM重建算法。
OSEM算法将投影数据分成N个子集,每次重建时只使用一个子集对投影数据进行校正,重建图像每更新一次,所有的子集都对投影数据校正一次,称为一次迭代[3]。和传统的迭代算法MLEM相比,在近似相同的计算时间和计算量下,重建图像被刷新了N倍,大大加快了图像重建速度,缩短了重建时间。

图5 OSEM法将投影数据分成多个子集
下图是PET扫描 (低计数)临床投影数据的OSEM重建结果及与MLEM和FBP结果的对比[1]。OSEM可在提升图像质量的情况下,大大缩短计算时间。因此,OSEM是目前应用最为广泛的PET重建技术。
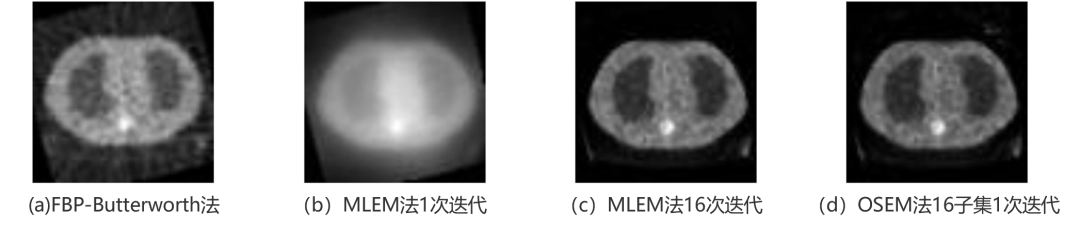
图6 不同重建算法效果对比
另外,迭代重建算法还可以根据具体成像条件,引入与时间、空间几何或测量值大小有关的约束条件,如飞行时间(TOF)、点扩散函数(PSF)、散射校正、衰减校正、噪声模型等[4-7],来进一步提升重建效率和图像质量。